|
闭口系统热力学第二定律 |
|
|
热力学第一定律只说明能量在传递和转换时的数量关系。热力学第二定律则要解决过程进行的方向、条件和深度等问题。其中最根本的是关于过程的方向问题 若一个系统经过一个准平衡过程,由始态变到终态,又能经过逆向过程由终态变到始态,不仅系统没有改变,环境也恢复原状态,即在系统和环境里都不留下任何影响和痕迹,这种过程在热力学中称为可逆过程。否则称为不可逆过程 可逆过程必为准平衡过程,而准平衡过程则是可逆过程的条件之一。对于不平衡过程,因为中间状态不可能确定,当然是不可逆过程 于是,热力学第二定律可表述为:一切自发地实现的过程都是不可逆的 熵是从热力学第二定律引出的,是一个状态参数 熵用符号S(s)表示,其定义为: dS= dQ/T (J/K) (式1-1) 1kg气体的比熵为: ds = dq/T (J·kg-1·k-1) (式1-2) 在可逆过程中熵的增量等于系统从外界传入的热量除以传热当时的绝对温度所得的商 |
|
|
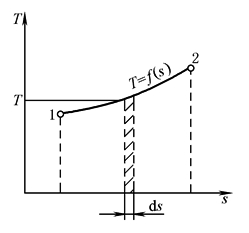
熵的作用可从传热过程和做功过程对比看出。在表闭口系统热力学第一定律p-V图上,功是过程曲线下的面积。同样,可作T-s图,如右图所示。图中曲线1-2代表一个由状态1变到状态2的可逆过程,曲线上的点代表一个平衡状态。在此过程中对工质加入的热量为:
可见,在T-s图上,过程曲线下的面积就代表过程中加入工质的热量。s有无变化就标志着传热过程有无进行 从式1-2知,当工质在可逆过程中吸热时,熵增大;放热时,熵减小。因此,根据工质在可逆过程中熵是增大还是减小,就可判断工质在过程中是吸热还是放热。若系统与外界绝热,dq=0,则必有ds=0,即熵不变,这样一个可逆的绝热过程称为等熵过程 |
T-s图 |
|
对于完全气体,比熵变化只与始态和终态参数有关,与过程性质无关,故完全气体的熵是一个状态参数 在不可逆过程,总的比熵的变化应等于系统从外界传入的热量以及摩擦损失转化成的热量之和除以传热当时的热力学温度所得的熵。由于存在摩擦损失转换的热量,不可逆的绝热过程是增熵过程,即ds>0 |
|