|
闭口系统热力学第一定律 |
|||
|
能量 |
含 义 |
符号及单位 |
|
|
热力学第一定律确定了各种形式的能量(热能、功、内能)之间相互转换关系,该定律指出:当热能与其他形式的能量进行转换时,总能量保持恒定。对于任何系统,各项能量之间的一般关系式为 进入系统的能量-离开系统的能量=系统中储存能量的变化 |
|||
|
热 量 |
由于温度不同,在系统与外界之间穿越边界而传递的能量称为热量。热量是通过物体相互接触处的分子碰撞或热辐射方式所传递的能量,其结果是高温物体把一部分能量传给了低温物体。热量传递过程并不需要物体的宏观运动。热量是过程量,不是状态参数 |
Q——热量,J或kJ W——功,J或kJ |
|
|
功 |
系统与外界之间通过宏观运动发生相互作用而传递的能量称为功 |
||
|
|
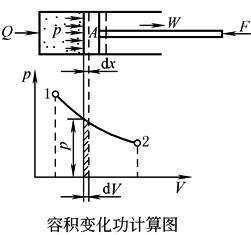
左图所示气缸中,密闭一定质量M的气体,可动边界活塞的面积A,活塞所受外力F。当系统克服外力进行一s个准平衡的膨胀过程,即由状态1变到状态2时,若不计摩擦,系统对外所做的功为:
在p-V图上,功是过程曲线下的面积。可见,即使始态、终态相同的两个过程,若过程曲线不同,功的大小也不同,这说明功不是状态参数而是一个过程量 |
||
|
内
能 |
气体内部的分子、原子等微粒总在不停地运动,这种运动称为热运动。气体因热运动而具有的能量称为内能,它是储存于气体内部的能量 对于完全气体,分子间没有相互作用力,内位能为零,完全气体只有内动能。这时内能只是温度的单位函数。1kg气体的内能称为比内能 U=f(T) 在气体的状态一定时,内能也有一定值,因而内能也是气体的状态参数 |
u——比内能,J/kg或kJ/kg U——内能,J或kJ q——1kg工质与外界变换的热量,J/kg或kJ/kg |
|
|
闭口系统的能量 平衡方程式 |
上图所示气缸中密闭一定质量气体的系统为闭口系统。设系统由状态1变到状态2为一个准平衡过程,在此过程中系统吸热量为Q,膨胀对外做功W,系统内能变化ΔU。对于这种闭口系统,热力学第一定律可表述为:给予系统的热量应等于系统内能增量与对外做功之和。热力学第一定律方程式的微分形式为: dQ=dU+dW 对1kg气体而言,有 dq=du+dw=du+pdυ |
||
|
焓 |
焓H的定义为 H=U+pV 1kg气体的比焓h的定义为 h=u+pυ=u+RT 在气动系统中,压缩空气从一处流到另一处,随着压缩空气移动而转移的能量就等于它的焓。当1kg气体流进系统时系统获得的总能量就是其内能u与1kg气体的推动功pυ之和,即为比焓h 在u、p、υ为定值时,h亦为定值,故焓为一状态参数 |
H——焓 h——比焓 |
|